Опубликована в журнале
Проблемы экспертизы в медицине, 2006, №2, с.58-60.
УДК 340.67:543.544
С.С.
Катаев, Н.Б. Зеленина
СМЕРТЕЛЬНОЕ ОТРАВЛЕНИЕ СМЕСЬЮ ЦИКЛОГЕКСАНОЛА И ЦИКЛОГЕКСАНОНА
Пермское областное бюро судебно-медицинской экспертизы (нач. бюро - В.И. Перминов)
Резюме
Описан случай
смертельного отравления человека смесью циклогексанола
и циклогексанона. Определены концентрации циклогексанола и циклогексана в содержимом желудка 456,5 и
414,9 мг/л, в крови 402,7 и 17,9 мг/л, в моче 262,9 и 20,1 мг/л. Употребление последних может быть
подтверждено определением в моче продуктов их метаболизма циклогександиолов.
При остром отравлении смесью циклогексанола и циклогексанона их метаболиты (циклогександиолы)
обнаруживаются в моче в неконъюгированном виде.
Ключевые слова: циклогексанол,
циклогексанон, газовая хроматография, газовая
хроматография – масс-спектрометрия.
S.S.
Kataev, N.B. Zelenina
MORTAL
POISONING by MIXTURE CYCLOHEXANOL and CYCLOHEXANONE
Summary
The
case of the mortal poisoning human by mixture cyclohexanol and cyclohexanone is
described. The concentrations cyclohexanol and cyclohexanone in gastric the contents 456,5
and 414,9 mg/l, in blood 402,7 and 17,9 mg/l, in urine 262,9 and 20,1 mg/l were determined. Use last can be confirmed by determination in
urine of the products of their metabolism cyclohexandioles.
In the case of the mortal poisoning by mixture
cyclohexanol and cyclohexanone,
its metabolites (cyclohexandioles) were detected in
urine in unconjugated type.
The keywords: cyclohexanol,
cyclohexanone, gas chromatography, gas chromatography
- mass-spectrometry.
Циклогексанол - бесцветные кристаллы со слабым
запахом камфоры и сивушного масла, Тпл 25,1оС, Ткип
161,1оC. CAS – [108-93-0]. Растворим в воде (4,3% по
массе при 20°С), смешивается с большинством органических растворителей,
растворяет многие масла, воски и полимеры. Получают гидрированием фенола, окислением
циклогексана (в этом случае обычно в смеси с циклогексаноном)
и др. способами. Применяют как растворитель и полупродукт в
производстве капролактама [2, 10].
Циклогексанон
- бесцветная жидкость с резким, напоминающим ацетон запахом, Тпл - 32,1°С, Ткип 155,6°С. CAS – [108-94-1]. Растворяется в воде (порядка 9,9% по объему
при 20°С), смешивается с большинством органических растворителей, растворяет
нитроцеллюлозу, ацетаты целлюлозы, жиры, воски, многие природные смолы,
поливинилхлорид и др. В промышленности получают каталитическим окислением
циклогексана (обычно образуется смесь с циклогексанолом) и каталитическим
окислением циклогексанола. Применяют главным образом как растворитель и
полупродукт для получения капролактама и адипиновой
кислоты [2, 10].
В
литературе отсутствуют сведения о смертельных отравлениях человека
циклогексанолом или циклогексаноном. Все данные
сводятся к изучению маркеров метаболизма данных соединений, как результата
воздействия паров последних на человека [6-8]. Описан один случай
комбинированного отравления составом, содержащим циклогексанон
[9]. Изучение острой токсичности циклогексанола на животных показывает [3], что
при оральном приеме LD50 для крыс
2,06 г/кг. Минимальная летальная доза для кроликов при введении через рот между
2,2 и 2,6 г/кг.
В нашей практике наблюдался случай
смертельного отравления человека смесью циклогексанола и циклогексанона
вследствие употребления её вовнутрь.
Оборудование.
Хроматограф Кристалл-2000, с модульным детектором ПИД
½, ЭЗД, ПФД (Россия). Генератор водорода и компрессор ("Хроматэк", Россия). Термоблок ПЭ-4030
("Экрос", Россия). Газовый хроматограф Agilent 6850, капиллярная кварцевая
колонка НР-5MS длиной 30 м
с внутренним диаметром 0,25 мм и толщиной пленки 0,25 мкм. Масс-селективный
детектор Agilent 5973N ("Agilent", США).
Материалы.
Растворители и реактивы градации х.ч. БСТФА
с 1% ТМХС (SIGMA Chemical Co., США).
Методы.
Результаты расчетов логарифма коэффициента распределения октанол/вода (LogP) получены с
использованием
"ACD/I-Lab service" (Advanced Chemistry Development Inc., Toronto,
Canada) по программе ACD/LogP
v4.5.
Метод определения летучих растворителей: 2 мл биожидкости или крови,
5 г мозга помещали во флаконы
объемом 10 мл, закрывали резиновой пробкой.
После фиксации пробки
к горловине флаконы
нагревали в термоблоке при 80оС
в течение 10 мин, по 2
мл парогазовой фазы
каждой пробы вводили подогретым
стеклянным шприцем в испаритель
хроматографа. Регистрация хроматограмм проводилась на
ПЭВМ. С целью количественного
определения к 2 мл крови или биожидкости
прибавляли 1 мл водного раствора н-пропанола с
концентрацией 4 мг/мл. Исследование на наличие летучих растворителей и
количественное определение ацетона проводили по изложенному ранее методу [1],
увеличив время анализа для колонки с неподвижной жидкой фазой «Carbowax-1500» до
11 минут. При этом время удерживания для циклогексанона
составило 7 мин 53 с, для циклогексанола
9 мин 37 с. Для колонки с
носителем «Porapak-Q» время удерживания для циклогексанола составило 16
мин 11 с, для циклогексанона 16 мин 28 с.
Условия количественного определения циклогексанола и циклогексанона.
К 2 мл
крови или биожидкости во флаконе объемом 10 мл
прибавляли 1 мл водного раствора н-пропанола с
концентрацией 4 мг/мл, флакон
закрывали резиновой пробкой.
После фиксации пробки
к горловине флаконы
нагревали в термоблоке при 80оС
в течение 10 мин, по 2
мл парогазовой фазы
каждой пробы вводили подогретым
стеклянным шприцем в испаритель
хроматографа. Детектор пламенно-ионизационный. Колонка металлическая длиной 2 м
и диаметром 0,3 см, заполненная сорбентом «Chromaton-N» с 5% неподвижной жидкой фазы «Carbowax-1500». Температура колонки программируемая
80оС в течение 1 мин, затем нагревание со скоростью 10оС/мин
до 140оС. Общее время анализа 7 мин. Температура испарителя 210оС.
Температура детектора 240оС. Скорости потоков: газа носителя - азота
60 мл/мин, водорода 120 мл/мин, воздуха 600 мл/мин. Регистрацию хроматограммы проводили на ПЭВМ. При этом времена
удерживания составили: н-пропанол – 1 мин 31 с; циклогексанон 4 мин 22 с; циклогексанол
5 мин 44 с. Калибровочную кривую строили по водным растворам циклогексанола и циклогексанона. Использовали стандарт циклогексанона
в воде с концентрациями: 20; 100; 500; 1000 мг/л. Стандарт циклогексанола
в воде с концентрациями: 200; 500; 1000 мг/л. Для каждой концентрации стандарта
проводили по три определения по выше изложенному методу.
Метод определения метаболитов циклогексанола.
Извлечение без гидролиза: К 1 мл мочи
добавляли хлорид натрия до насыщения. Экстрагировали однократно 5 мл
этилацетата. Экстракт выпаривали в токе теплого воздуха.
Извлечение после гидролиза: К 1 мл мочи добавляли 1 мл 6 н. раствора соляной кислоты, укупоривали и выдерживали в течение 1 ч при 100оС. Гидролизат охлаждали, насыщали хлоридом натрия. Экстрагировали однократно 5 мл этилацетата. Экстракт выпаривали в токе теплого воздуха.
Дериватизация.
К сухому остатку в виале прибавляли 100 мкл БСТФА с 1% ТМХС, пробу укупоривали и выдерживали в течение 1 ч при 80оС. После охлаждения 1 мкл образца вводили в инжектор ХМС.
Режим работы автосамплера:
·
три промывки этанолом;
·
три промывки этилацетатом;
·
одна промывка шприца раствором пробы;
·
три прокачки раствором пробы перед вводом;
·
набор и ввод пробы;
·
три промывки этанолом;
·
три промывки этилацетатом.
Режим работы ХМС.
Скорость потока
газа-носителя (гелий) через колонку 1,5 мл/мин, режим работы split/splitless (деление потока
1:15, с задержкой включения 1 мин после
ввода пробы). Температура инжектора и
интерфейса 250 и 280оС, температура колонки - градиент 50оС
в течение 5 мин, затем прогрев до 280оС со скоростью
программирования 6оС в 1 мин, выдержка при конечной температуре 5
мин. Регистрация масс-спектров в режиме
полного сканирования масс 45-450 а.е.
Обсуждение результатов
На
исследование был предоставлен биологический материал от трупа гражданина Г. с
диагнозом: отравление неизвестным ядом. Со слов родственников выпил порядка 80 мл
ацетона. На исследование были доставлены: кровь, печень, ткани головного мозга,
125 мл мочи, желудок с содержимым
(содержимое желудка - 60 мл кашицеобразной массы серого цвета с фрагментами
пищи).
При
исследовании крови и биожидкостей методом газожидкостной
хроматографии были обнаружены ацетон, циклогексанон и
циклогексанол. Результаты количественной оценки
содержания обнаруженных веществ приведены в таблице 1.
Таблица 1.
Количественное
содержание ацетона, циклогексанона, циклогексанола в биологическом материале.
|
Соединение |
Содержимое
желудка, мг/л |
Кровь, мг/л |
Моча, мг/л |
|
Ацетон |
34,5±4,4 |
44,5±2,8 |
27,2±1,5 |
|
Циклогексанон |
414,9 ±
33,0 |
17,9 ±
0,3 |
20,1 ±
1,0 |
|
Циклогексанол |
456,5 ±
30,7 |
402,7 ±
44,6 |
262,87 ±
0,02 |
При
этом в тканях мозга на качественном уровне найдены
ацетон и циклогексанол.
На колонке «Porapak-Q» при совместном присутствии циклогексанол
и циклогексанон не разделяются. Как дополнительное
подтверждение было использовано выявление метаболитов циклогексанола в моче
методом ХМС.
Метаболизм
циклогексанола приведен на рисунке 1. Основное направление метаболизма
циклогексанола (1) обусловлено образованием сульфатов и глюкоуронидов,
с последующим выведением конъюгатов с мочой [3], а
так же гидроксилированием с образованием
1,2-циклогександиола (2), 1,3-циклогександиола (3), 1,4-циклогександиола (4)
[5]. Период полувыведения циклогексанола составляет около 12 часов. Циклогексанон метаболизирует с
образованием циклогексанола. Дигидроксипроизводные
циклогексана 1,2- и 1,4- циклогександиолы рассматриваются как маркеры
экспозиции паров циклогексана, циклогексанона и циклогексанола на человека [6-8].

Рис.1.
Метаболизм циклогексанола. Циклогексанол
(1), 1,2-циклогекандиол (2), 1,3-циклогекандиол (3), 1,4-циклогекандиол (4).
Учитывая низкую
липофильность дигидроксипроизводных
циклогексана (таблица 2) при их извлечении органическим растворителем из мочи,
применяли хлорид натрия для увеличения эффективности экстракции.
Таблица 2.
Коэффициенты
распределения октанол/вода (logP) для циклогександиолов.
|
Соединение |
Расчет |
Литературные
данные |
|
цис-1,2-Циклогександиол |
0,15±0,24 |
0,23 [4] |
|
транс-1,2-Циклогександиол |
0,15±0,24 |
0,08 [4] |
|
цис- и транс-1,3-Циклогександиолы |
-0,29±0,21 |
Нет
данных |
|
цис- и транс-
1,4-Циклогександиолы |
-0,08±0,21 |
Нет
данных |
Для разрушения сульфатов и глюкоуронидов использовали кислотный гидролиз. На
определяемое количество цис-1,3- циклогександиола кислотный гидролиз повлиял
мало, а количественный выход цис- и транс-1,2- циклогександиолов значительно увеличивается
(рисунок 2). Специфика выведения циклогександиолов обусловлена фактором липофильности. Менее липофильные
1,3- и 1,4-циклогександиолы выводятся в основном в нативном
виде, а более липофильные 1,2-циклогександиолы
частично подвергаются конъюгации. Вследствие гидролиза наблюдается увеличение
фона балластных веществ, существенно затрудняющих идентификацию определяемых
компонентов по их масс-спектру, в особенности транс-1,3-, цис- и транс-1,4- циклогександиолов.
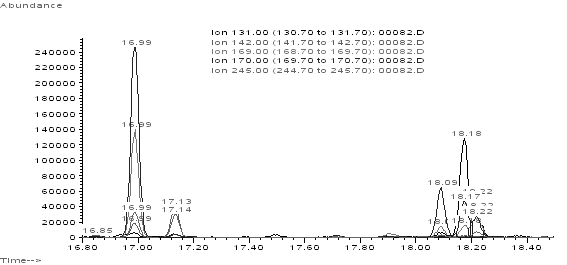
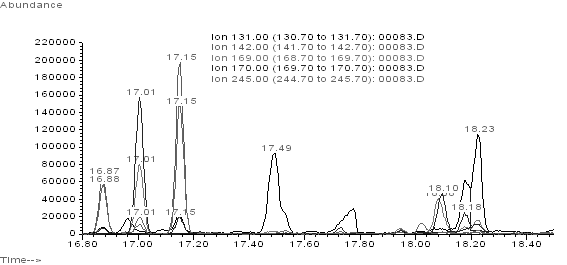
Рис.2.
Экстракционные хроматограммы профилей мочи без
гидролиза (сверху) и после кислотного гидролиза (снизу). Времена удерживания бис-ТМС эфиров (сверху): цис-1,3-циклогекандиола – 16,99
мин, цис-1,2-циклогекандиола – 16,85 мин, транс-1,2-циклогекандиола – 17,13
мин, транс-1,3-циклогекандиола – 18,09 мин, цис-1,4-циклогекандиола – 18,18
мин, транс-1,4-циклогекандиола – 18,22 мин. Времена удерживания бис-ТМС эфиров (снизу): цис-1,3-циклогекандиола – 17,01
мин, цис-1,2-циклогекандиола – 16,87 мин, транс-1,2-циклогекандиола – 17,15
мин.
Идентификацию
циклогександиолов в виде триметилсилиловых
эфиров проводили с помощью масс-спектральных библиотек NIST98, WILEY275 и по
данным работы [5]. Хромато-масс-спектрометрические характеристики триметилсилиловых эфиров циклогександиолов
приведены в таблице 3.
Таблица
3.
Хромато-масс-спектрометрические
характеристики триметилсилиловых (ТМС) эфиров циклогександиолов.
|
Соединение |
Характеристические
ионы m/z, а.е.
(интенсивность, %) |
tуд., мин. |
|
цис-1,2-Циклогександиол,
бис-ТМС эфир |
147
(100); 73 (62); 142
(59); 245
(43); 81 (29); 129
(28); 75
(18); 148 (16); 133 (14);
149 (14); 155 (10) |
16.85 |
|
цис-1,3-Циклогександиол,
бис-ТМС эфир |
170 (100); 169 (53); 73 (50); 75 (38); 155 (26); 217 (20); 116 (18); 171 (18); 115 (14); 245 (13); 101 (11); 129 (11); 147 (11) |
16.99 |
|
транс-1,2-Циклогександиол,
бис-ТМС эфир |
147
(100); 73 (69); 142 (67); 245
(44); 129 (30); 81 (29); 75
(21); 148 (16); 133 (14); 149
(14); 155 (13); 45 (11); 143 (10) |
17.14 |
|
транс-1,3-Циклогександиол,
бис-ТМС эфир |
81 (100);
147 (85); 170 (63); 73 (49); 217 (47); 116 (32); 149 (28); 75 (27); 155 (17);
101 (16); 129 (14); 148 (14); 169 (14); 133 (13); 171 (10) |
18.09 |
|
цис-1,4-Циклогександиол,
бис-ТМС эфир |
131
(100); 81 (75); 73 (48); 147
(36); 170 (33); 75 (26); 149
(18); 169 (15); 155 (14); 132
(12); 133 (12) |
18.18 |
|
транс-1,4-Циклогександиол,
бис-ТМС эфир |
73 (100);
131 (92); 169 (75); 170
(53); 75 (51); 147 (20); 155
(20); 245 (17); 45 (10); 74
(10); 132 (10) |
18.22 |
Описан случай исследования,
выполненного при отравлении человека смесью циклогексанола и циклогексанона. Употребление последних может быть подтверждено
определением в моче продуктов их метаболизма циклогександиолов. При остром
отравлении смесью циклогексанола и циклогексанона их метаболиты (циклогександиолы)
обнаруживаются в моче в неконъюгированном виде.
Литература
1. Катаев С.С. // Проблемы экспертизы в
медицине. 2004.- №4.- C.51-52.
2. Химическая энциклопедия. Т.5. М.: «Большая Российская энциклопедия», 1998.
3.
Evidence on the developmental and reproductive toxicity
of cyclohexanol. DRAFT, 2001. Reproductive and Cancer
Hazard Assessment Section Office of Environmental Health Hazard Assessment
4. Hansch C., Leo A.J. Substituent
constants for correlation analysis in chemistry and biology. Wiley:
5. Mills G.A.,
Walker V. // Clin.
Chem. 1990.- Vol.36.- N.6.- P.870-874.
6. Mraz J,
Galova E, Nohova H, et al. // Int. Arch. Occup. Environ.
Health. 1994. - Bd. 66. - N.3. S.203-208.
7. Mraz J,
Galova E, Nohova H, et al. // Int. Arch. Occup. Environ.
Health. 1998. - Bd. 71. - N.8. S.560-565.
8. Mraz J, Galova
E, Nohova H, et al. // Scand. J.Work. Environ. Health. 1999. Vol.25. N.3. P.233-237.
9. Sakata M,
Kikuchi J, Haga M, et al. // J.
Toxicol. Clin. Toxicol. 1989. Vol.27.
N.1-2. P.67-77.
10. The Merck Index: An Encylopedia of Chemicals, Drugs, and Biologicals;
12th Edition.
Катаев
Сергей Сергеевич
E-mail: forenschemist@narod.ru